計算と物理的解釈
水素原子の電子軌道を計算したときにはエネルギー準位は主量子数だけで決まってしまうという結果を得た.ところが水素以外の多電子原子では電子どうしの相互作用を考慮しないといけないのでそれほど単純な結果にはならない.方位量子数
やスピン状態
によってもエネルギーに違いが出てくることになる.
磁気量子数による違いは出ないのか?と思うかもしれないが,外部から磁場が掛かっていなければ気にしなくていい.方位量子数
は全角運動量の絶対値を決めているパラメータであり,磁気量子数
はその
軸成分を表している.つまり,
というのはもし観測したならばその角運動量ベクトルがどの方向を向いているかというような違いを表しており,全体から見ればどの方向も対等なのである.わざわざ観測しない限りは
の値の異なる複数の状態が重なり合う形になって存在していることだろう.それがどのような割合で重なり合っているかは一個一個の原子それぞれで違っていてもいい.
原子内の一つの電子の がある値になっていることによって影響を受けて,同じ原子内の別の電子のエネルギーに違いが出るということは起こり得るだろう.つまり,その別の電子というのは最初の電子の
の値によって決まるエネルギー最低の状態を取って安定することになる.ところが原子全体の向きを変えて見てやれば最初の電子の
の値は違って(あるいは重なって)見えるのであり,結局どこか一つの電子の
の値が幾つになっていようとも,全体としては向きが違うだけのエネルギー的には何ら違いのない状態のいずれかに落ち着くことになるのである.
いきなり脱線したが,元の話に戻そう.方位量子数やスピン
の違いによって生じるエネルギー差というのはごく僅かなものだが,主量子数が大きいところではその僅かな差によってもエネルギー準位の順序が入れ替わるようになってくる.主量子数
の値が大きくなるほどエネルギー準位の間隔が狭くなっていくことを思い出そう.
実際,元素を原子番号順に並べた電子配置の一覧表を見ると,単純に K 殻,L 殻,M 殻の順に電子が埋まっていくわけではないことが分かる.高校の頃の自分はそれを見て気持ち悪さを感じていた.なぜエネルギーの低いところから順に埋まっていかないのだろう?と.今にして思えば,疑問の持ち方が間違っていた.電子はエネルギー準位の低い方から順に軌道を埋めていくのだが,その順序はもはや主量子数だけでは決まらないというだけのことである.
そのような状況を考慮した方程式を作ることはそれほど難しくはない.難しいのは出来上がった方程式を解く作業であり,人力ではほとんど不可能である.ではどうするかというと,思い切り設定を単純化して近似的な手法で対処するか,コンピュータを使った数値計算に頼ることになる.
方程式の作り方は単純である.電子どうしの電荷の反発力や,角運動量やスピンによって生じる磁気モーメントのエネルギーをハミルトニアンに入れてやればいいだけである.古典力学の知識を使って得られる式をそのまま演算子に置き換えて素直に当てはめればいい.
これを知った時のガッカリ感と言ったら!量子力学を学び始めたばかりの頃の自分は量子力学に過度な期待をしていた.電子がもはや波として存在するのなら,それらの相互作用のメカニズムは波のイメージを使って説明されるに違いないと信じていたのである.古典力学では説明されなかった「離れた電荷どうしに働く力」の正体がもっと根本的なレベルから説明されると思っていたし,古典力学では起こりえない現象も出てくるのだろうと思っていた.後者については間違いではなかったが,思っていたのとはずいぶんイメージが違った.古典力学の式をそのまま使って導いた結果に満足しろだなんて.
今の私はその頃と比べるとずいぶん考え方が変わった.古典力学の結果をハミルトニアンに代入して解くだけ,なのではなく,相互作用のハミルトニアンがそのような形で表せるような世界になっていることの方が根本的な事実であり,古典力学的な現象はそれを反映して起きているだけなのではないだろうか,と.この考えは場の理論まで考えるようになるとますます強まってくる.相互作用も含んだハミルトニアンの形が,時空の対称性から自然に定まってくるように思えるからだ.物理現象は機械装置的な仕組み(素朴実在論)で説明されるようなものではなく,かなり数学寄りの時空の対称性から説明されるものであって,我々は現実的な物体や形やそのようなものが存在するのだと錯覚しているだけなのかもしれない.今はこの話はこれくらいにしておこう.
さて,方程式を立てて,それを解くことが出来て,その結果として得たものがどれも現実の現象と寸分違わないものならば,我々の仮定は正しかったことになる.実際,コンピュータの性能も計算手法もどんどん進歩して,そのような比較検証が可能になってきている.
数値計算の結果が現実と合うならばそれこそが全てでありそれで十分なのかもしれないが,人間というのはもっと理解しやすい直観的な解釈も欲しくなるものである.あまりに単純な直観的な解釈というのは時には成り立たないこともあるのだが,役に立つこともある.少し条件を変えた場合にどんな結果になるかを素早く推測するための指針になったりするからだ.条件が少し変わるたびに計算し直すのは面倒なものだから,ちょっとやそっとでは覆らないような解釈があればとても助かる.
その定性的な解釈が妥当と言えるかどうかを検証するのも面白い.当初は妥当だと誰もが信じたような説明が後の細かな検証で突き崩されたという例もいっぱいある.
以下では,電子軌道に電子が埋まっていく順を説明するための,おそらく正しいと思われる定性的な解釈を紹介することにしよう.
この記事を仕上げるための参考として手に入れた『入門分子軌道法』という教科書の前書きにも似たような注意が書かれていた.理論があまりに美しいためにその通りのことが実際にそのまま起きているのだと思い込んでしまう「ピグマリオン症」というものに陥らないように気を付けなさいというものである.

『入門 分子軌道法』 (藤永 茂 著)
マーデルング則
実は電子が軌道を埋めていく順序については次のような視覚的に分かりやすい法則がある.
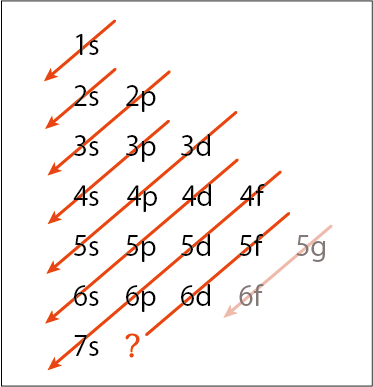
上の矢印から順に,矢印に従うように軌道が埋まっていくというのである.
3p 軌道まではこんな図に頼らなくても良さそうである.まず主量子数の小さい軌道が優先されて,主量子数が同じ場合には軌道量子数
の小さい軌道が優先されていると考えるだけで説明が付きそうだ.この単純な法則は原子番号 18 番のアルゴンまで通用する.
しかしそれ以降は番狂わせが起こる.なぜか 3d 軌道に行かず,上の図のように先ず 4s 軌道を埋めることが優先されるのである.
さて,この図のような法則が常に成り立つかと言えばそうではない.時々例外が起こる.例外の話を始めると面倒になるので後にしよう.多少の例外があるものの,このような分かりやすい法則が成り立つのは面白い.何か理論的な根拠がありそうだ.
ところがそれほど数学的にしっかりとした根拠があるわけではないのだ.最後の方の 5f と 6d ではどちらが優先されるのか怪しくなってくる.6d が先に 2 個だけ埋まった後,6d が 1 個だけに戻って 5f が埋まり始めたりする.そして,どちらも完全に埋まることなく原子番号 92 番のウランに到達して天然元素についてはこれで終わりだ.
理科年表にはウラン以降の人工元素の電子配置も載っている.そこまで視野に入れると,5f より 6d が先に埋まり始めるのは僅かな例外と言ってもいいような気もしてくる.5f が完全に埋まった後で 6d が比較的順調に埋まって行き,なんと,この図には書かなかった 7p が理論通りに埋まり始めるところまで載っている.
5g や 6f が薄く描かれているのは,結局それらの軌道は理論上は存在するが使われないで終わるので,この法則が成り立っているかどうかすら確かめようがないという理由である.多分,かなり破綻しているところがあるのではないかと思う.
この図のような法則が何と呼ばれているか,良くわからない.「構造原理」や「増成原理」と呼んでいる事例は見たことがある.どちらも訳し方が違うだけで元の単語はドイツ語混じりの aufbau principle という単語である.しかしこの用語の意味を調べてみると「電子はエネルギーの低い準位の軌道から順番に埋まっていく」という現代から見ればごく当たり前の内容を指しているものらしい.昔はこういう基本的なことすらも「有力な仮説」として扱われていたのだろう.
もう少し調べてみたら「マーデルング則」あるいは「マーデルングの規則」というのが正式な名称だということが分かった.
現時点で「"構造原理"原子」で検索すると約 7000件のヒットがあるが,「マーデルング則」や「マーデルングの規則」の検索結果を合計しても 10 件しかない.またWikipediaの「電子殻」の項を見ると,この規則を表す図が「増成原理」というタイトルで紹介されている.日本語ではこの用語はあまり使われていないようである.
遮蔽効果
マーデルング則が成り立つ理由を考えてみよう.先ほどの図を描き直すと,こういうことでもある.
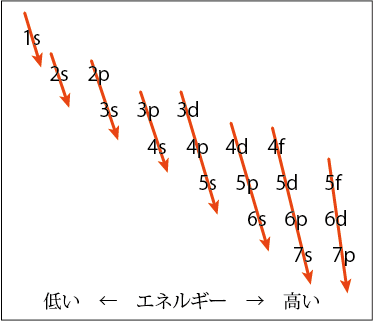
最初は矢印が縦一直線になるようにきっちり一つ分ずつスライドさせてみようと思っていたが,もう少しだけ多めにずらせば左から順に埋まっていくという感じが演出できるのではないかと気付いてそうした.
主量子数によるエネルギーの違いが左右の位置のズレとして表されているが,方位量子数
によるエネルギーの違いも左右に幅があり,その度合いがたまたまうまい具合に一つずつのズレで収まるくらいになっているということのようである.
ではなぜ,方位量子数によるエネルギーの違いが s < p < d < f の順になるのだろうか?全角運動量が小さい方がエネルギーが低い……?実際そうなっているようだが,もしそういうことが言えるのならば水素原子の場合でもそういう結果が出たはずだ.しかし水素原子の場合には主量子数だけでエネルギーが決まっており,角運動量の違いは関係してこないのだった.何か他の理屈を探した方が説得力があるだろう.
そこで,電子軌道の形に注目する.1s 軌道は球対称であり,中心が最も存在確率が高く,中心から離れるほど徐々に薄れていく雲のように分布している.そのような先客がいるところに 2s 軌道に入るのと 2p 軌道に入るのと一体どちらが楽であるかを考えてみよう.
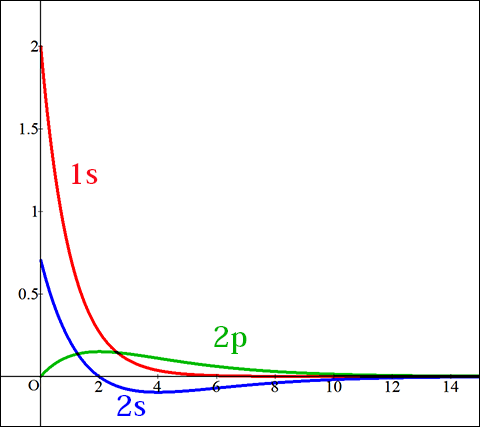
2s 軌道も球対称であり,中心から少し離れたところで一度確率が薄くなり,1s 軌道より広く外側へと分布しているが,やはり中心付近の確率密度が最も高いような形をしている.2p 軌道は亜鈴型の分布をしているのだが,そのような形状はひとまず考慮から外すと,中心から離れたところに存在確率のピークがある.
直観的には 2p 軌道を選んだ方が 1s 軌道の濃い雲を避けることが出来て電子どうしの反発の影響が少なくなる気がする.電子どうしが近付きすぎるとポテンシャルエネルギーは高くなってしまうから 2s より 2p の方がエネルギーが低いのではないだろうか.ところが直観というのは時々頼りにならなかったりもする.別の直観でこれとは逆の結論を導いてみせよう.
1s 軌道というのは電子がビュンビュン飛び回っているのではなく,全体的に同時に確率的に存在しているのである.さて,地球に深い穴を掘って中心付近をくり抜いて大空洞を作ってやると,その内部では無重力になるという,ニュートン力学で有名な例題を思い出してほしい.外側にある球殻状の質量から均等に引かれるために,内部では重力を少しも感じないでいられるのである.2s 軌道ではこれと同じ効果が起きる.中心付近ではあたかも自分より外側に分布する 1s 軌道の電子の雲が存在しないかのような状況となっているのだ.よって,原子核の引力だけをもろに感じて,強く引き寄せられる結果となる.
一方,2p 軌道はより外側の 1s 軌道電子の存在確率が薄まったところに多く分布している.外側から見れば原子核の電荷を 1s 電子が均等に薄ぼんやりと覆ってしまっている感じになっており,引力をそれほど強く感じることが出来ない.これを「遮蔽効果」と呼ぶ.このため,束縛がゆるくなり,エネルギー準位が浅くなるのである.
実際に 2s 軌道の方がエネルギーが低いことから,後者の直観の方がより現実を正しく説明できるようだ.
他の軌道の遮蔽効果
遮蔽効果によって s 軌道より p 軌道の方が束縛が緩くなるのだろうという話をしたが,d 軌道や f 軌道ではどうなっているだろうか?
その話の前に,先ほどのグラフについて少し反省をしておこう.あれは水素原子の場合に解いて求めた「動径分布関数」をそのままグラフにしたものである.実際の存在確率は波動関数の絶対値の 2 乗であるし,規格化のための定数も,全空間で積分したときに 1 になるように調整してある.だから先ほどのグラフの面積は軌道ごとに違ってしまっている.印象操作の疑い「有り」なのだ.
存在確率の合計は,次のように球面調和関数と一緒にした上で,波動関数の絶対値の 2 乗を作って,全空間で積分して 1 になるように調整している.
幸いにして動径
に依存する部分と方向
に依存する部分が綺麗に分離できているので,
については次の関係を満たすように規格化しておけばいいのである.
先ほどのグラフもこのような条件を満たす規格化定数を使っているのだが,グラフ上ではあまり意味を成していない.代わりに次のように
を縦軸にしてグラフにするとどの軌道の面積も 1 になって,存在確率の分布を比較しやすいだろう.
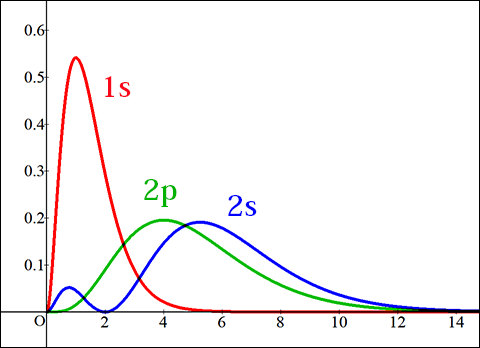
横軸は半径である.このグラフは「ある半径
のところに電子がある確率」を意味していることになる.1s 軌道は中心付近が一番確率密度が高いはずなのだが,このグラフでは中心から離れたところにピークが来ている.それはなぜかと言えば,半径が大きい領域の方が体積が広いから,そちらで見出される可能性の方がより大きくなるということである.2s 軌道の存在確率がが中心を離れたところで一旦 0 になって再び盛り上がっていることもよく分かるようになっている.
こうして見ると 2p 軌道より 2s 軌道の方が外側にあるように思えるのだが,1s 軌道の外側にあるということではどちらも大差はない.注目すべきは,2s 軌道の一部が原子の中心付近にわずかな瘤を持っており,それが 1s 軌道のピークより内側にあるというところである.
さて,同じような意味で描かれた 3s,3p,3d 軌道のグラフを見てみよう.
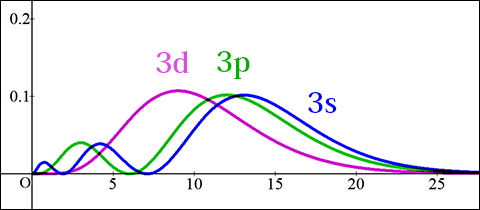
横軸のスケールが変わっていることに注意して比べてみれば 2s や 2p よりずっと外側まで確率が広がっていることが分かるだろう.中でも 3s 軌道が一番外側まで広がっている.しかし 3s 軌道は 1s 軌道のピークよりもかなり内側にもわずかなピークを持っている.3p 軌道も中心からは少し離れているが 1s 軌道に重なるようにある程度の存在確率がある.残る 3d 軌道は一番内側に近いように見えるが,かなり外側でやっと唯一のピークを持つ.このようなわけで s 軌道が最も強く引かれ,1s 軌道のずっと外側にある 3d 軌道は他の電子に遮蔽されて中心の電荷をあまり感じないのである.
どの軌道がどの程度の遮蔽効果を受けているのかについては,この解釈が実験データと合うように,いわば「後付け」で数値が決められている.
最後に,重要な注意をしておこう.ここまで,いかにも水素原子について計算した電子軌道の形がそのまま存在するかのように説明をしてきた.実際には電子軌道の形も変わっている可能性があるのであって,かなり定性的な説明であることを覚えておこう.
話がかなり長くなってしまったので一旦ここで休憩しよう.例外的にマーデルング則に従わない原子では何が起こっているのかという話は次回にしたい.










